Durch die wissenschaftlichen Erkenntnisse der letzten 10 Jahre ist heute klar, dass Wale Paarhufer sind – mit erstaunlichen Anpassungen an ihre aquatische Umwelt
Von STEFAN HUGGENBERGER
Institut II für Anatomie, Universität zu Köln, 50924 Köln
Email: st.huggenberger@uni-koeln.de
Zusammenfassung:
 Die moderne Forschung zeigt, dass Wale zur Ordnung der Paarhufer (Artiodactyla) gehören, auch wenn sie erstaunliche Anpassungen an ihren aquatischen Lebensraum zeigen. Die Bartenwale besitzen einen Filterapparat aus Hornlamellen im Oberkiefer, der sie so erfolgreich im Nahrungsnetzwerk der Ozeane macht, dass sie Riesenformen entwickelten. Ihre Schwestergruppe, die Zahnwale hingegen entwickelten ein Echoortungssystem, mit dem sie Fische und Tintenfische in völliger Dunkelheit jagen können. Der größte Vertreter der Zahnwale, der Pottwal, jagt mittels Echoortung in dunklen Tiefen von 800 m und mehr. Um die Beute in dieser großen Tiefe akustisch zu orten hat er ein feines Gehör und eine extrem laute Stimme. Zahnwale generieren den Schall jedoch mit Hilfe der Nase und nicht wie andere Säugetiere mit dem Kehlkopf. Die Nase ist beim Pottwal besonders beeindruckend: Sie besteht in erster Linie aus zwei riesigen Fettkörpern, so dass mehr als ein Viertel des Gesamtgewichts von großen Pottwalen dem Gewicht der Nase zuzuschreiben ist. Mit ihrer Schallkanone in der Nase generieren Pottwale die lautesten Vokalisationen im Tierreich und sind damit die Super-Jäger (Apex-Predatoren) der Tiefsee.
Die moderne Forschung zeigt, dass Wale zur Ordnung der Paarhufer (Artiodactyla) gehören, auch wenn sie erstaunliche Anpassungen an ihren aquatischen Lebensraum zeigen. Die Bartenwale besitzen einen Filterapparat aus Hornlamellen im Oberkiefer, der sie so erfolgreich im Nahrungsnetzwerk der Ozeane macht, dass sie Riesenformen entwickelten. Ihre Schwestergruppe, die Zahnwale hingegen entwickelten ein Echoortungssystem, mit dem sie Fische und Tintenfische in völliger Dunkelheit jagen können. Der größte Vertreter der Zahnwale, der Pottwal, jagt mittels Echoortung in dunklen Tiefen von 800 m und mehr. Um die Beute in dieser großen Tiefe akustisch zu orten hat er ein feines Gehör und eine extrem laute Stimme. Zahnwale generieren den Schall jedoch mit Hilfe der Nase und nicht wie andere Säugetiere mit dem Kehlkopf. Die Nase ist beim Pottwal besonders beeindruckend: Sie besteht in erster Linie aus zwei riesigen Fettkörpern, so dass mehr als ein Viertel des Gesamtgewichts von großen Pottwalen dem Gewicht der Nase zuzuschreiben ist. Mit ihrer Schallkanone in der Nase generieren Pottwale die lautesten Vokalisationen im Tierreich und sind damit die Super-Jäger (Apex-Predatoren) der Tiefsee.
Noch am Ende des letzten Jahrhunderts war das Wissen über Walfossilien so spärlich, dass man nicht sicher sein konnte, wie die Vorfahren der Wale (Cetacea) aussahen. In den letzten 25 Jahren hat sich das Blatt entscheidend gewendet. Heute ist sicher, dass Wale zu den Paarhuftieren (Artiodactyla) zählen, die erstaunliche und einzigartige Anpassungen an ihren aquatischen Lebensraum zeigen. Hierbei brachte der Filterapparat aus Barten im Oberkiefer den heutigen Bartenwalen (Mysticeti) einen entscheidenden Vorteil im Nahrungsnetzwerk der Ozeane. Barten sind Hornlamellen, die im Maul der Wale ein Reusensystem bilden. Damit „filtern“ sie große Mengen an Planktonkrebsen und kleineren Fischen aus dem Wasser. Bartenwale sind also, obwohl sie sich von kleinen Beutetieren ernähren, eher als Weidegänger zu bezeichnen (Abb. 1). Dieses Konzept der Ernährung mittels der Barten war in der Evolution offensichtlich so erfolgreich, dass die Vertreter der Bartenwale die größten Tiere stellen, die auf unserer Erde leben. Der Blauwal ist das größte Tier, das je gelebt hat.

Mit Echolot in die Tiefe
Ihre Schwestergruppe, die Zahnwale (Odontoceti) hingegen haben eine andere Taktik des Nahrungserwerbs gefunden. Mit ihrer Echoortung erjagen sie größere Beutetiere. Sie senden aktiv Klicklaute aus, deren Echo vom Tier gehört und in ein „akustisches Bild“ der Umwelt umgesetzt wird. So können Zahnwale mit der Echoortung Fische und Tintenfische in völliger Dunkelheit jagen. Damit sie ihre schnelle Beute erwischen, sind die wendigen Zahnwalvertreter meist weit kleiner als die großen Bartenwale und, wie z.B. die Delphine, zu akrobatischen Leistungen fähig. Der großte Vertreter der Zahnwale, der Pottwal (Physeter macrocephalus), hat seine ökologische Nische hingegen in der Tiefsee gefunden. Er jagt im Mesopelagial, oft weit mehr als 200 m unter dem Meeresspiegel. Pottwale sind an der Oberfläche nur Gäste, um sich mit dem lebenswichtigen Sauerstoff zu versorgen und sich von ihren Jagdausflügen in die Tiefe zu erholen. Um die Beute in der großen Tiefe zu orten, reicht das Echolot der Pottwale über viele hundert Meter. Das der Delphine funktioniert nur im Nahbereich erfolgreich (bis ca. 115 m).
Für die Echoortung ist ein feines Gehör und eine laute Stimme Voraussetzung. Schon die Vorfahren aller heutigen Wale zeigten Anpassungen des Gehörs an das Leben unter Wasser. Die ersten Urwale (Archaeoceti) mit stark reduzierten Hinterbeinen zeigten Ohrknochen, die fast gänzlich vom Schädel abgekoppelt waren (Abb. 2). Dadurch konnten Mittelohr- und Innenohrstrukturen frei vom Rest des Schädels schwingen und ermöglichten so ein stark verbessertes Richtungshören unter Wasser1.
Die entscheidende Entdeckung machten die Paläontologen Philip Gingerich und Donald Russell (University of Michigan) 1981 im trockenen Sand und Gestein von Pakistan. Sie fanden in etwa 53 Millionen Jahren alten Süßwassersedimenten eine vierbeinige, amphibisch lebende Übergangsform, Pakicetus inachus, die unverwechselbar mit den Walen verwandt war. Die winzigen Gehörknöchelchen Hammer, Amboss und Steigbügel sind in einer knöchernen Kapsel an der Unterseite des Schädels eingeschlossen aber nur bei Walen ist der Rand der Ohrkapsel zur Mitte hin extrem dick und hoch mineralisiert. Dieser Zustand findet sich schon bei Pakicetus.
Wale sind Paarhufer
Dann, im Jahr 2001, beschrieben zwei Forscherteams, eins um J.G.M. ‚Hans‘ Thewissen (heute Northeast Ohio Medical University) und ein weiteres um Philip Gingerich, die maßgebenden Skelettfunde der Pakicetus-Verwandtschaft. Gattungen wie Ambulocetus, Remingtonocetus, Rodhocetus und Protocetus dokumentieren eine Zugehörigkeit der Gruppe der Urwale zu den Paarhuftieren. Ein Knochen im Fußgelenk der fossilen Urwale, das Rollbein (Talus) hat die typische Form einer „Umlenkrolle“ (Trochlea). Dieses Merkmal weist eindeutig nach, dass Wale und Huftiere eine gemeinsame Ordnung bilden und somit monophyletisch miteinander verwandt sind.
Moderne Studien aus dem Bereich der Molekularbiologie zeigen ein passendes Bild: Die Aminosäure-Sequenzen lebender Wale sind am ehesten mit Paarhufern wie Antilopen, Schweine und Hirsche zu vergleichen. Es zeigte sich, dass die evolutionäre Beziehung der heutigen Wale innerhalb der Paarhufer am nächsten zu den rezenten Nilpferden steht. Die Ergebnisse sind also eindeutig: Wale sind Paarhuftiere. Um die Zusammengehörigkeit der beiden taxonomischen Gruppen der Cetacea und der Paarhufer (Artiodactyla) zu dokumentieren, wird die zusammengefasste Ordnung in modernen Lehrbüchern als Cetartiodactyla bezeichnet.
Obwohl nicht eine Reihe von direkten Vorfahren, so stellt jede Gattung der bisher erforschten Urwalfossilien ein bestimmtes Stadium der Walevolution dar. Gemeinsam zeigen sie, wie der Übergang vom Land zum Wasserleben stattfand (Abb. 3). Die frühesten bekannten Urwale, wie Pakicetus und der etwas ältere Himalayacetus, waren mehr auf dem Land zu Hause als im Wasser. Sie haben wahrscheinlich in Seen und Flüssen im „Hunde-Paddel-Stil“ ihrer Beute aufgelauert. Rund eine Million Jahre später lebte Ambulocetus, ein früher Wal im Erscheinungsbild wie ein Krokodil mit großem Schädel und großen Füßen mit Schwimmhäuten. Der langschnäuzige Remingtonocetus erschien neben der kleineren Form Kutchicetus in der flachen Umgebung von Salzwassermooren.

Etwa zur gleichen Zeit wie Remingtonocetus lebten Formen wie Protocetusund Rodhocetus ihr ganzes Leben im Meer. Diese vollständige Anpassung in den maritimen Lebensraum erlaubte es diesen Urwalen, ihre Reichweite zu den Ufern anderer Kontinente zu erweitern. Es entstanden schlankere, schnelle Schwimmer wie Basilosaurus oder Dorudon, die die warmen Meere des späten Eozän bevölkerten.
Bartenwale mit und ohne Barten
Die Jäger der eozänen Ozeane starben schließlich aus, aber nicht ohne dass sich ihre Verwandtschaft in die heutigen Zahnwale und Bartenwale entwickelte. Die frühen Vertreter dieser Gruppen erschienen vor etwa 33 Millionen Jahren (Abb. 3). Die ersten Bartenwale, wie z.B. die Gattung Aetiocetus, hatten noch keine Barten, sondern besaßen Zähne. Durch das große Vorkommen der Planktonkrebse im Oligozän konnten einige Bartenwalvorfahren eine Filtertechnik entwickeln, die darauf beruhte, dass die Backenzähne mit vielen Spitzen ausgestattet waren. So bildeten die Zähne des Ober- und Unterkiefers zusammen ein Gitter, in dem sich die Krebse verfingen und dann geschluckt wurden. Um das Zahngitter zu unterstützen kamen später wahrscheinlich die Barten dazu. Die Zähne verloren so ihre Funktion, so dass sie noch im Bartenwalfötus angelegt werden, beim Neugeborenen aber nicht mehr zu sehen sind.
Moby Dicks Schallkanone
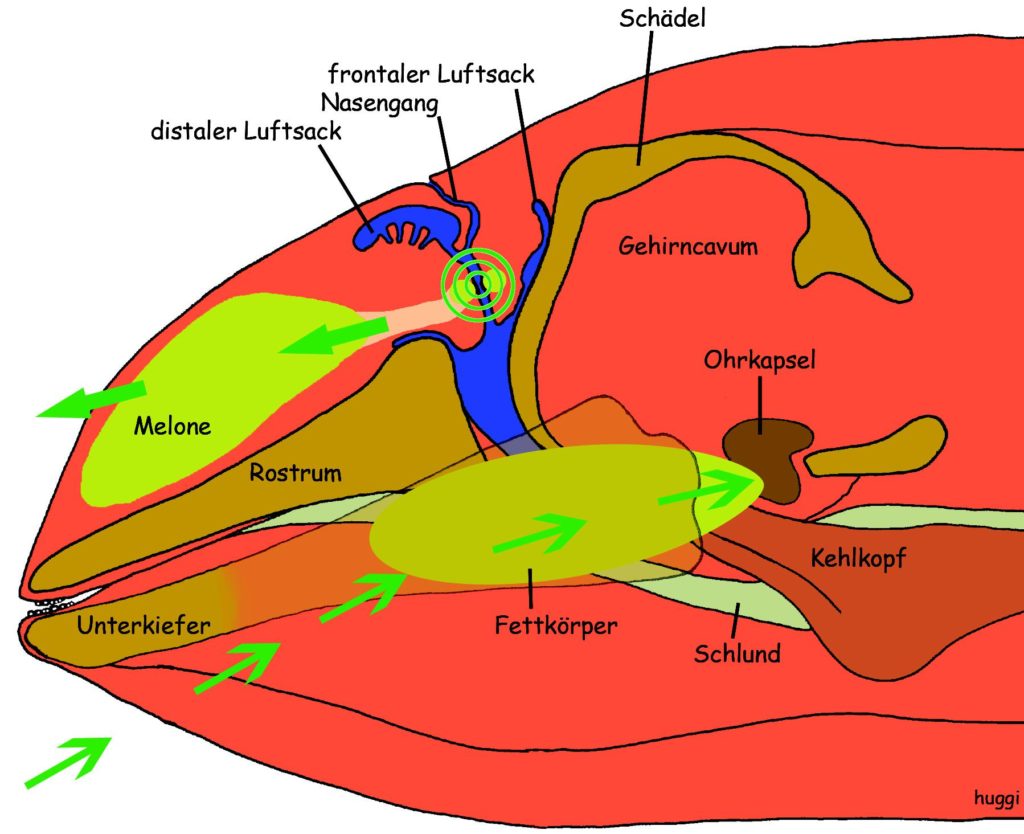
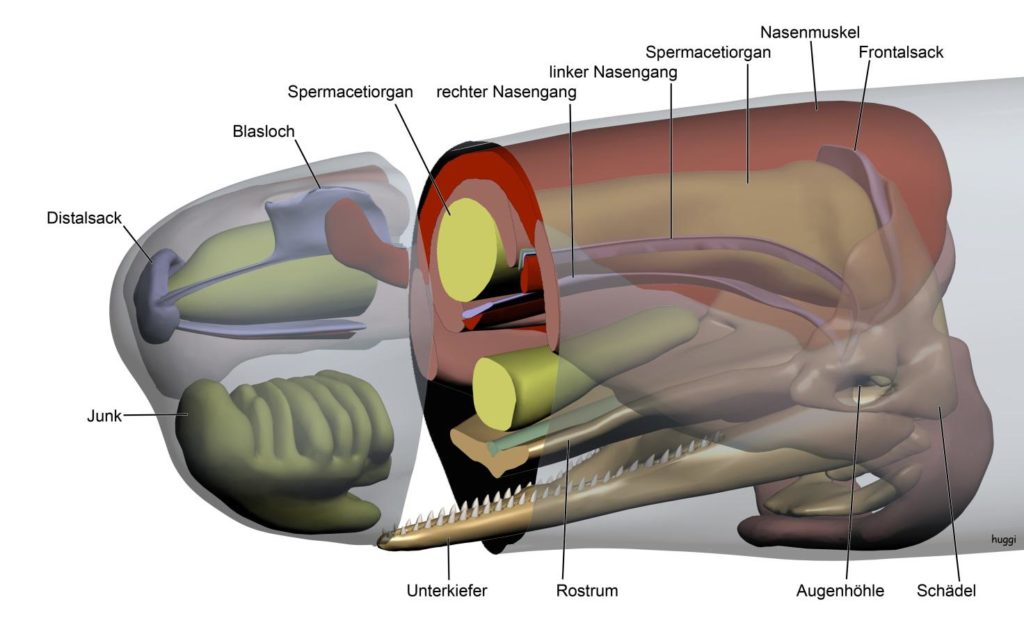
In etwa parallel zu der Entwicklung der Barten, entstand bei Zahnwalen ein System der Echoortung. Wie oben erwähnt, senden sie Klicklaute aus, deren Echo Informationen zum Aussehen ihrer Umwelt liefert. Um unter Wasser ohne nennenswerten Verlust von Energie Schall zu erzeugen und fokussiert auszusenden, evolvierte ein hypertropher Komplex in der Nase dieser Tiere (Abb. 2). Delphine und andere Zahnwale generieren den Schall also in der Nase und nicht, wie bei anderen Säugetieren üblich, mit dem Kehlkopf. Beim Pottwal ist die Nase besonders beeindruckend: Der Nasenkomplex degradiert den Schädel zu einer insignifikant kleinen Struktur. Dabei ist der Schädel von 18 m großen Pottwalbullen alleine schon fast 6 m lang. Er bildet einen Sessel in dem der Nasenkomplex sitzt (Abb. 4). Dieser wird in erster Linie von zwei riesigen Fettkörpern gebildet so dass mehr als ein Viertel des Gesamtgewichts von großen Pottwalen dem Gewicht der Nase zuzuschreiben ist. Mit seiner Schallkanone in der Nase generieren Pottwale den lautesten Schall im Tierreich – bis zu 236 dB re. 1 µPa, was in Luft theoretisch 205 dB ergeben würde. Mit diesen Lautstärken lassen sich sogar die Weiten der Tiefsee akustisch erkunden. Jagdausflüge bis in dunkle Tiefen von 800 m und mehr sind keine Seltenheit. Wahrscheinlich hält der Pottwal auch mit einer Tiefe von 3 km den Tiefenrekord aller mit Lungen atmenden Tiere. Im Pelagial, dem freien Tiefenwasser unserer Ozeane, lauert er dann seiner Beute auf. Möglichst große Tintenfische stehen dabei ganz oben auf der Liste. In der Tiefe ist der Pottwal zusammen mit einigen kleineren Schnabelwalarten ein konkurrenzloser Jäger. Keine andere Tierart jagt in diesen Tiefen mit Hilfe der Echoortung, die dank der extrem lauten Nasen-Schallkanone über weite Strecke einsetzbar ist.
Die Laute der Pottwale dienen aber nicht nur der Echoortung sondern auch der Kommunikation. Feine Unterschiede in der Klickstruktur zeigen, ob ein Pottwal einen Kommunikationsklick oder einen Echoortungsklick aussendet. Ein Kommunikationsklick besteht aus einer Serie von kurzen Pulsen, während ein Echoortungsklick idealerweise aus nur einem einzelnen lauten Puls besteht. Die Multipulsstruktur der Kommunikationsklicks wird dadurch erzeugt, dass die initiale Schallwelle mehrere Male im Nasenkomplex hin und her reflektiert wird, indem die Luftfüllung der Nasengänge modifiziert wird.
Kultur der Rhythmen
Kommunikation spielt im sozialen Leben der Pottwale eine große Rolle. Sie leben meist in Herden (Schulen) von bis zu 30 Tieren, die über weite Strecken akustisch in Verbindung bleiben können. Diese Schulen bestehen entweder aus einigen Weibchen mit ihrem Nachwuchs oder aus einer Gruppe junger Männchen. Alte Bullen wiederum leben allein und treffen nur sporadisch auf Artgenossen. Durch ihren höheren sozialen Rang sind es jedoch diese alten Bullen, die bei der Fortpflanzung den größeren Erfolg haben. Dieses komplexe Sozialsystem der Pottwale begründet sich auf bestimmte Rhythmen der Kommunikationsklicks, die sich Coda (ital. la coda, le code – Schwanz, Schweif) nennen – ein Begriff aus der Musik entlehnt. Die Bedeutungen dieser Code sind im Einzelnen noch nicht geklärt. Jedoch zeigen nur bestimmte geographische Gruppen bestimmte Kombinationen von Code, die von den Artgenossen erlernt werden müssen. Dies weist sehr stark auf einen kulturellen Zusammenhang zwischen verschiedenen Kommunikationsformen (Codatypen) und geographischen bzw. familiären Beziehungen hin.
Referenzen und weiterführende Literatur:
Gingerich PD, ul Haq M, Zalmout IS, Khan, IH, Malkani MS. 2001. Origin of whales from early artiodactyls: Hands and feet of eocene Protocetidae from Pakistan. Science 293: 2239–2242.
Huggenberger S, André M, Oelschläger HHA. 2014. An acoustic valve within the nose of sperm whales Physeter macrocephalus. Mammal Review 44:81–87.
Huggenberger S, André M, Oelschläger HHA. 2014. The nose of the sperm whale: overviews of functional design, structural homologies and evolution.Journal of the Marine Biological Association of the UK (First View):1–24.
Price SA, Bininda-Emonds ORP, Gittleman JL. 2005. A complete phylogeny of the whales, dolphins and eventoed hoofed mammals (Cetartiodactyla).Biological Review 80: 445-473.
Switek B. 2010. How did whales evolve?http://www.smithsonianmag.com/science-nature/how-did-whales-evolve-73276956/?no-ist.
Thewissen JGM, Williams EM, Roe LJ, Hussain ST. 2001. Skeletons of terrestrial cetaceans and the relationship of whales to artiodactyls. Nature 413: 277–281.
Westheide W, Rieger G. (Eds.) 2015. Spezielle Zoologie. Bd.2, Wirbeltiere. 3. neubearbeitete Auflage. Heidelberg: Spektrum Akademischer Verlag.
Whitehead H. 2003. Sperm Whales: Social Evolution in the Ocean. University of Chicago Press.
Kommentare erwünscht
Wollen Sie diesen Text kommentieren? Dann schicken Sie uns einen Leserbrief, den wir an dieser Stelle veröffentlichen werden.


Leserbrief zu: Wale – Paarhufer im Wasser (26.03.2016)
Der lesenswerte Artikel „Wale – Paarhufer im Wasser“ von Dr. Stefan Huggenberger hat einen sehr zu begrüßenden Überblicks- und Einführungscharakter. Zu einigen Details möchte ich dennoch Anmerkungen machen, die hilfreich sein können.
Kapitel „Mit Echolot in die Tiefe“:
Der Urwal Pakicetus inachus wurde nicht „1981 im trockenen Sand und Gestein von Pakistan“ durch Gingerich und Russell entdeckt. Vielmehr haben diese Autoren 1981 eine Studie über das Fossil vorgelegt. In Pakistan gefunden wurde es bereits 1979 von Jean-Louis Hartenberger. Es ist auch nicht 53 Millionen Jahre alt, wie Stefan Huggenberger sagt: Diese Zahl bezieht sich in Wirklichkeit auf einen anderen Fund (Himalayacetus subathuensis), bei dem aber keine Ohrknochen erhalten sind.
Kapitel „Wale sind Paarhufer“:
Pakicetus war noch mehr ein Water als ein Paddler. Indem von einem Lauerjäger die Rede ist, wird in die Textdarstellung bereits der spätere Ambulocetus hineingemischt.
Abbildung 3: Frühste Neoceti (Zahn- und Bartenwale) entstanden nicht erst im Oligozän, wie die Bildbeschriftung sagt, sondern bereits am Ende des Eozän, so Llanocetus denticrenatus. Aber etliche frühe Familien von Zahn- und Bartenwalen sind in der (schon etwas älteren) Abbildung gar nicht aufgeführt. Dort verwundert, dass unter holozänen Zahnwalen die Platanistidae in denselben Ast gestellt werden wie die Iniidae und Lipotidae, während die Pontoporiidae einem ganz anderen zugeordnet werden, und zwar praktisch als Teil der modernen Delphinoidea.
Laut Text des Artikels „lebten Formen wie Protocetus und Rodhocetus ihr ganzes Leben im Meer. Diese vollständige Anpassung in den maritimen Lebensraum […].“ Damit erhebt Huggenberger die genannten Vertreter der Protocetidae bereits in die Reihen der sogenannten Pelagiceti, die sich völlig vom Land gelöst hatten. Tatsächlich aber konnten Protocetus und Rodhocetus noch auf den Strand kriechen und waren darauf wohl, etwa zum Gebären, auch noch angewiesen. Sie hatten sich noch nicht auf ein reines Wasserleben spezialisiert.
Kapitel „Bartenwale mit und ohne Barten“:
Hier stellt der Artikel ein Gitter aus großen Zähnen bei frühen „Bartenwalen“ (Mysticeti) vor, die noch keine Barten entwickelt hatten. Dann heißt es: „Um das Zahngitter zu unterstützen kamen später wahrscheinlich die Barten dazu.“ Diese Formulierung impliziert, dass es zunächst ein Zusammenwirken von Zahngitter und Barten gab. Doch Ende 2015 (Monate nach dem Huggenberger-Artikel) erklärte eine neue Studie, dass ein Zusammenwirken von Barten und großen Zähnen kaum funktioniert haben dürfte. Bevor die Barten entstanden, entwickelte sich nach heutiger Anschauung dickes Zahnfleisch, das eine saugende Aufnahme der Nahrung in den Mundraum förderte. Erst als die Zähne kleiner wurden, scheinen Barten aufgetreten zu sein.
Kapitel „Kultur der Rhythmen“:
Über die Kommunikation der Pottwale heißt es: „Jedoch zeigen nur bestimmte geographische Gruppen bestimmte Kombinationen von Code […].“ Unklar ist an dieser Stelle, was genau gemeint ist: der Aufbau innerhalb eines Codatyps (z.B. mit einem zeitlich abgesetzten Schlussklick bei sogenannten „+ 1 Codas“), oder aber das Repertoire aus unterschiedlichen Codatypen, das eine bestimmte Walgemeinschaft benutzt. Eine geographische Trennung zwischen zwei „Sprachgruppen“ (vocal clans) ist für den Pazifik-Bereich als eine Besonderheit vor Japan festgestellt worden. In östlicheren Pazifik-Bereichen gibt es eine solche geographische Trennung nicht. Genau das aber unterstreicht umso mehr den kulturellen Charakter der Unterschiede zwischen den verschiedenen Pottwalgruppen.
Diese Anmerkungen, die keinen Anspruch auf Vollständigkeit erheben, mögen das Verständnis des guten Artikels von Stefan Huggenberger und den Umgang damit erleichtern und verbessern.
Literatur:
Johannes Albers (2015, Erstfassung 2003): Die frühen Urwale Indopakistans. Ein Überblick über die wichtigsten Formen und ihre Erforschung. – Cetacea.de/Palaeocetologie. http://www.cetacea.de/palaeocetologie/indopakistan/Albers_Indopakistan_2015.pdf
Masao Amano, Aya Kourogi, Kagari Aoki, Motoi Yoshioka und Kyoichi Mori (2014): Differences in sperm whale codas between two waters off Japan: possible geographic separation of vocal clans. – Journal of Mammalogy 95/1: 169-175.
Felix G. Marx, Cheng-Hsiu Tsai und R. Ewan Fordyce (2015): A new Early Oligocene toothed ´baleen´ whale (Mysticeti: Aetiocetidae) from western North America: one of the oldest and the smallest. – Royal Society Open Science 2: 150476.
Redaktioneller Hinweis:
Zwei weitere Hinweise von Johannes Albers zur Arbeitsstätte von J.G.M. Thewissen und zur Benennung der Ziphiidae waren Anlass, diese Stellen im Artikel von Stefan Huggenberger zu korrigieren.