Vortrag mit Demonstrationen
Prof. Dr. Klaus Wächtler
Institut für Zoologie, Tierärztliche Hochschule Hannover
Vortrag am Mittwoch, 19. Januar 2005
an der Tierärztlichen Hochschule Hannover,
Hörsaal Anatomisches Institut
Zusammenfassung
-
- 1. Einleitung
- 1.1. Primäre und sekundäre Meerestiere
- 2. Wale
- 2.1. Herkunft und System
- 2.2. Bemerkungen zur Anatomie
- 2.2.1 Körperform
- 2.2.2. Haut
- 2.2.3. Größe
- 2.2.4. Skelett
- 2.2.5. Schädel
- 2.2.6. Gehirn
- 3. Walgehirne
- 3.1. Hirngewichte im Vergleich
- 3.2. Anatomie des Walgehirns
- 3.2.1. Übersicht über die Teilsysteme
- 3.2.2. Reduktion des Riechapparates
- 3.2.3. Geschmackssinn
- 3.2.4. Optisches System
- 3.2.5. Akustisches System
- 3.2.6. Weitere Besonderheiten
- 4. Schluss
- 4.1. Das Gegenbeispiel: Der niedrige Cephalisationsgrad der Seekühe
- 1. Einleitung
1. Primäre und sekundäre Meerestiere
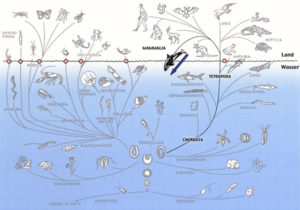
Die meisten Tiere sind primäre Meerestiere. Die erfolgreichsten Landbewohner sind die Insekten, Spinnentiere, einige Asseln, Lungenschnecken, Reptilien, Vögel und Säugetiere. Eine Rückwanderung ins Meer haben nur wenige Gruppen mehr oder weniger vollständig vollzogen (Abb. 1).
In dieser Tabelle, die noch um einige Insekten und Milben und aus der Gruppe der Tetrapoden um einen marinen Frosch, Rana cancrivora (Remmert 1992), zu ergänzen wäre, sind nur die Wale und die Seekühe reine Meerestiere geworden (Abb. 2). Alle anderen ernähren sich zwar im oder am Meer, können schnell schwimmen und tief tauchen, sind aber zumindest während der Fortpflanzung auf Landaufenthalte angewiesen.
An dieser Stelle soll es um Wale und deren Gehirne gehen. Davor aber noch einige Bemerkungen zu Bauplanbesonderheiten der Wale.
2. Wale
2.1. Herkunft und System

Die Wale sind vor ca. 60 Millionen Jahren im Alttertiär aus Vorfahren hervorgegangen, die sie mit den heutigen Paarhufern, insbesondere dem Flußpferd verbinden. Über kurzbeinige Stadien, die gewisse Ähnlichkeit mit Krokodilen hatten und im Bereich flacher Küsten lebten, sind sie zu Meerestieren geworden, die am Land nicht mehr leben können, obwohl sie Lungenatmer geblieben sind.
Sie sind rezent mit etwa 86 Arten in 40 Gattungen und 14 Familien vertreten und werden meist als zwei lange getrennte Unterordnungen, die Zahnwale (Odontoceti) und die Bartenwale (Mysticeti), an die Urwale (Archaeoceti) angeschlossen (Abb. 4). Eine wichtige Gemeinsamkeit dieser drei Gruppen ist der Bau der Ohrkapsel (Tympanoperioticum), die aus porzellanartigem Knochenmaterial besteht, bei den rezenten Walen von Fett- und Bindegewebspolstern umgeben wird und nicht mit dem Schädel verwachsen ist.
Da die Zähne bei allen Walen zumindest embryonal angelegt sein können, wird die Trennung zwischen Zahn- und Bartenwalen von einigen Taxonomen heute als weniger grundsätzlich angesehen. Nach Bewertung der zurzeit bekannten anatomischen, genetischen und biochemischen Übereinstimmungen schlägt Klima (2004) die Einteilung in 5 Gruppen“ (wohl Überfamilien) vor (Abb. 3)

2.2. Bemerkungen zur Anatomie
2.2.1. Körperform
Dass die Cetaceen im Volksmund Walfische heißen und dass manche U-Boote im Bugbereich Pottwalen ähneln, ist kein Zufall: Die Walform ist für die Fortbewegung im Wasser optimal. Die querstehende Schwanzflosse (Fluke) als kräftiges Antriebsorgan, die Rückenflosse (Finne) und eine riesige Ölwanne auf der Stirn, das Spermaceti-Organ oder die Melone (s.u.) sind in dem Zusammenhang nützliche Neubildungen ohne Entsprechungen im Säugetierbauplan.
2.2.2. Haut
Die straffe, elastische Walhaut mit den oberflächlich ineinandergreifenden Papillen und der darunter liegenden massiven Isolierschicht aus Fett minimiert Reibungsverluste durch Wirbelbildung und wird von Bionikern zu Recht bewundert. Das Fell, ein wichtiges Säugetierkennzeichen, ist bis auf wenige Haaranlagen reduziert. Als Folge davon sind auch die Ektoparasiten nicht mehr, was sie mal waren“. Während die Läuse im Robbenfell mit Hilfe einiger Anpassungen marine Insekten geworden sind, sind die wegen ihrer Klammerbeine äußerlich ähnlichen Walläuse“ marine Krebse.
2.2.3. Größe
Die Körperlänge der Wale liegt zwischen 1,50 m und 33 m. Also vom Menschenmaß bis zu einer schwimmenden Insel. Die Größenverhältnisse sind in Abbildung 8 dargestellt. Das Gewicht eines über 30 m langen Blauwals wird mit 130 Tonnen angegeben. Es entspricht z. B. dem Gewicht von vier Dinosauriern, 1600 Menschen oder 30 Elefanten.
2.2.4. Skelett
Im Skelett ist vieles anders als bei Landsäugetieren. Die ursprünglich bewegliche Verbindung zwischen Kopf und Rumpf wird starr. Die Vorderextremitäten mit oft verlängerten Fingern werden zu Flossen. Hinterextremitäten und Becken sind bis auf kleine, von der Wirbelsäule getrennte Reste reduziert. Ein einzelner Wirbel eines Finnwals aus dem mittleren Bereich der Wirbelsäule wiegt 16 kg. Mit einem solchen Skelett wird das Stranden zum Verhängnis.
2.2.5. Schädel
Der Schädel kann bis zu einem Drittel der Körperlänge ausmachen. Eine wichtige Veränderung, die sich am Schädel und auch an Ontogenesestadien schrittweise verfolgen lässt, ist die Verlagerung der Nasenöffnung vom Rostrum zum Scheitel. Dies hat vielfache Folgen für die Lagebeziehung der Schädelknochen zueinander, die statt hintereinander zunehmend übereinander angeordnet werden (Abbildung 10). Auf diese Weise entsteht ein abgeflachter, in der Breite auslaufender Hirnschädel (siehe Gegenüberstellung der Schädel von Fuchs und Tümmler). Die Nasengänge, die die Nasenöffnung im Schädel mit dem hochgelegenen Blasloch verbinden, sind streckenweise erweitert. Hier werden nicht nur in kräftigen Stößen große Luftmengen durchgeleitet, sondern auch Laute erzeugt, die der Kommunikation über weite Strecken sowie der Orientierung und Echoortung dienen. In der Mulde zwischen verlängertem Oberkiefer und Stirn liegt bei Pottwalen ein bis tonnenschwerer ölgefüllter Ballon, das erwähnte Spermacetiorgan (auch als Melone bezeichnet), welches beim Tauchen und Orten unterschiedlichste Funktionen erfüllt -nur nicht die, die man ihr mit der Phantasie der Küstenvölker ursprünglich zugeschrieben und im Namen festgelegt hat, nämlich die eines Spermienbehälters. Die Bezeichnung Sperm whale“ beruht auf diesem Irrtum.
Die gleichförmigen, meist konischen Zähne können in langen Reihen angeordnet oder bis auf einige Sonderbildungen reduziert sein. Die Ausbildung der Barten als senkrecht von den Gaumenrändern in die Mundhöhle ragenden Hornlamellen ist im Tierreich einmalig. Durch bogenförmige Aufwölbung des Oberkiefers und dem in seiner Höhe verstellbaren Mundboden entsteht bei den Bartenwalen eine Filtriereinrichtung von gigantischen Ausmaßen.
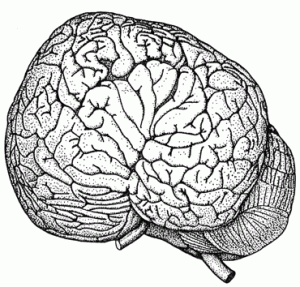
2.2.6. Gehirn
Während die bisher kurz betrachteten Sonderbildungen der Wale alle als Anpassungen an das Wasserleben zu erklären sind, ist die Vergrößerung des Gehirns seit Verlassen des Festlandes schwieriger zu begründen. Als zumindest ein wichtiger Impuls für die progressive Entwicklung des Gehirns insgesamt ist die Ausprägung eines leistungsfähigen Kommunikations- und Ortungssystems mit differenzierter Lauterzeugung und Schallwahrnehmung anzusehen. Das bestimmende Sinnesorgan ist das Gehör mit großräumiger zentraler Repräsentanz (s. u.).
3. Walgehirne
3.1. Hirngewichte im Vergleich
Gehirne bestehen aus großen Mengen kompliziert verschalteter Nervenzellen und aus ebenso großen Mengen die Neurone umgebender Gliazellen. Hinter einer Zunahme dieser Elemente in einem Gehirn kann man zu recht Funktionserweiterungen und Leistungssteigerungen erwarten. Unter bestimmten Bedingungen kann man bereits dadurch zu interessanten Einsichten kommen, dass man die im Detail komplizierteste aller Strukturen einfach auf die Waage legt. Daraus haben sich, auf den Menschen bezogen, vor allem im vorigen Jahrhundert, Tabellen ergeben, die im Zeitalter des ranking“ eine wahre Freude sind. Für Hannover ist die Tabelle von Kuhlenbeck aus dem Jahre 1927 die vorteilhafteste (Abb. 14). Hier liegen der Hannoveraner und seine Frau in Führung, weit vor Eskimos, Bayern, Sachsen und Österreichern. Noch schöner ist die Prominententabelle aus einer frühen Rauber-Koppsch-Auflage. Da liegen Cuvier vor Gauß und Schiller, Kant vor Bunsen und Haeckel. Und bei Mommsen aus Garding hätte es fast zum Hannoveraner gelangt (siehe auch Hagner 2004). Bezieht man Wale in diesen schlichten Wettbewerb mit ein, dann ist der Pottwal mit 9,8 kg nicht zu überbieten, während der Mensch irgendwo zwischen Elefant und Pferd einzustufen wäre. Um es kurz zu machen: Auskünfte über den Cephalisationsgrad vergleichbarer Tiergruppen lassen sich nur über die Hirngewicht- Körpergewicht- Beziehungen erzielen. Das heisst, wenn man berücksichtigt, dass der Pottwal mit dem größten Gehirn aller Zeiten einen Körper von der Größe eines Reisebusses versorgen muss, während der Mensch, ob nun Hannoveraner oder nicht, mit seinen ca. 1500 g ein Soma von hundert Kilogramm oder weniger koordinieren muss, fällt die Reihung deutlich anders aus. In der folgenden Tabelle sind einige Zahlenangaben zu Walgehirnen zusammengestellt (Abb. 16). In einer vergleichenden Grafik zum relativen Hirngewicht verschiedener Wirbeltiere wird der hohe Cephalisationsgrad der Wale, vor allem der Delphine, innerhalb der Säugetiere deutlich (Abb. 17). Auch wenn die Fähigkeit zu geplantem Handeln bei Walen unterschiedlich eingeschätzt wird, sind die Hirngewichts-Körpergewichtsbeziehungen von Cetaceen und Primaten nicht weit von einander entfernt.
3.2. Anatomie der Walgehirne und Sinnesorgane
Das Gehirn der Wale ist in der Dorsalansicht breiter als lang. Endhirn -und Kleinhirn sind lateral ausladend und die deutlich größten Teilsysteme. Genauere Zahlenangaben beziehen sich meist auf das Gehirn von Delphinen. Die Cortexoberfläche des stark gefurchten Telencephalon von Tursiops truncatus wird mit 3745 cm2 (Mensch 2275 cm2) angegeben. Die Dicke des Cortex beträgt beim Wal 1, 3 mm und beim Menschen 1, 8 mm. Daraus ergibt sich für das Cortexvolumen eines Delphins etwa 80 Prozent des menschlichen Cortex. Histologisch ähnelt der große Cetaceencortex dem basaler Insektivoren. Eine Lamina- IV-Region ist bei Cetaceen nicht abzugrenzen. Auf der Ventralseite gehört die Reduktion des Riechnerven und die Vergrößerung des Gehörnerven (s.u.) zu den auffälligsten Merkmalen.
Wie sich aus Untersuchungen an fossilen Walschädeln ergibt, zeichnet sich das große Cerebellum schon bei den Urwalen ab, während das Endhirn noch nicht annähernd das Volumen der rezenten Cetaceen zeigt. Bei Durodon (Archaeoceti) ist die Nasenöffnung noch rostral und ein Bulbus olfactorius noch vorhanden. (Abbildung 19). Auch in der Ontogenese sind diese frühen Zustände vorübergehend zu sehen, allerdings mit dem Unterschied, dass sich hier das Kleinhirn deutlich später entfaltet als das Telencephalon. Bulbus olfactorius, Riechnerv und Tractus olfactorius werden normal angelegt, Nasenöffnung und Telencephalon sind noch abwärts gerichtet. In späteren Stadien richtet sich das Telencephalon soweit auf, dass die Ventralseite nicht nach unten, sondern nach vorne zeigt.
Die volle Reifung des Gehirns dauert bei Tursiops einige Jahre. Das Gehirngewicht von ca. 1500 g ist bei der Geburt zu 42 %, nach 18 Monaten zu 80 % und nach fünf bis zehn Jahren zu 100 % erreicht. Die Asymmetrie des Schädels mit mehr oder weniger deutlicher Verstärkung der Strukturen auf der rechten Seite lässt sich zumindest bei einigen Delphinen auch am Gehirn zeigen, ohne dass sich dies bislang schlüssig erklären ließe. Denkbar sind Zusammenhänge mit dem Richtungshören. Noch interessanter sind vorübergehende Asymmetrien in der Hirnfunktion. Bestimmte EEG- Befunde deuten darauf hin, dass Delphine in Ruhephasen wahlweise eine Hemisphäre abschalten können.
Geruchssinn
Während die peripheren Teile des Riechapparates bei Zahnwalen ganz verschwinden, bleibt der Tractus olfactorius sichtbar. Interessant ist aber, dass zentraler gelegene Anteile des Riechhirns, wie Tuberculum olfactorium und Septumkerne bei allen Walgehirnen erhalten bleiben. Ein feiner Nervus terminalis bleibt ebenfalls nachweisbar. Die Riechnervreduktion wirkt sich auch auf den Schädelbau aus, wie der Vergleich eines Tümmlers mit dem eines Makrosmatikers, z. B. einem Reh oder einem Rind, zeigt. Über die Ausprägung des Geschmacksinnes gibt es unterschiedliche Einschätzungen. Geschmacksknospen an der Delphinzunge in fünf bis acht V-förmigen Vertiefungen sind zwar nachweisbar, aber ohne deutliche Nervenversorgung. Gehirnnerven VII und IX sind nicht reduziert und ein entsprechender Thalamuskern ist ebenfalls vorhanden. Einige Dressurversuche deuten darauf hin, dass Delphine in der Lage sind, im Wasser gelöste Stoffe zu unterscheiden.
Optisches System
Bis auf weitgehende Reduktion bei Flussdelphinen (der Gangesdelphin ist so gut wie blind) sind die Augen der Cetaceen gut entwickelt. Besonders bei tieftauchenden Arten sind sie zum Schutz vor großem Druck von kräftigen Bindegewebskapseln umgeben. In der Retina sind sehr große Ganglienzellen mit starken Fortsätzen weit verbreitet. Die optische Projektion von der Retina verläuft offenbar ausschließlich kontralateral. Der Nervus occulomotorius ist eher schwach entwickelt. Der laterale Kniehöcker im Zwischenhirn hat keinen Schichtenbau. Im Mittelhirn ist der Nucleus superior (optisches Projektionsgebiet) kleiner als der Nucleus inferior (akustisches Projektionsgebiet). Der visuelle Cortex im Endhirn liegt nicht- wie sonst bei Säugetieren üblich- am Occipitalpol, sondern weiter vorn.
Akustisches System
Die starke Entwicklung des akustischen Systems ist ein wichtiger Impuls sowohl für die Vergrößerung des Walgehirnes insgesamt als auch für die Ausbildung des Cortex. Im Vergleich zur Situation beim Menschen sind im Delphingehirn die Stationen der Hörbahn deutlich vergrößert: der mediale Kniehöcker ist siebenmal so stark, der Colliculus inferior zwölfmal und der laterale Lemniscus 250-mal so stark. Der VIII. Hirnnerv ist mehrfach so stark wie der des Menschen. Das Gehörorgan enthält die für Säugetiere typischen Bestandteile. Das Hören unter Wasser wird aber durch einige Spezialisierungen verbessert. Dazu gehört die Unterbringung der Rezeptoren in einer Kapsel, die andere Schwingungseigenschaften hat als die Schädelknochen. Dieses Ohrskelett (Petrosum und Tympanicum) ist aus schwerem porzellanartigem Knochenmaterial aufgebaut und vom Schädel durch Fett und Bindegewebshüllen abgesetzt. Die Schallleitung entsteht bei Zahnwalen über den Unterkiefer, insbesondere eine Zone dünneren Knochens (pan bone), der den Schall an den im Unterkiefer eingebetteten Fettkörper überträgt. Dieser leitet die Schallwellen bis ans Ohr. Die Gehörknöchelchen und Trommelfell sind ähnlich denen der Landsäuger ausgebildet. Die Zahnwale haben ein Sonarsystem. Dies gibt es offenbar bereits bei den Squaolodontiden im Oligozän, aber noch nicht bei Durodon. Sie können Töne im Bereich von 20 bis 150 kHz hören und aussenden. Nach Ansicht einiger Beobachter werden die ausgesandten Ultraschalltöne durch die Melone gebündelt. Die Leistungen diese Echoortungssystems sind erstaunlich. Von Tursiops wird berichtet, dass er 10 cm große Metallkugeln auf 150 m Entfernung nicht nur orten, sondern auch unterscheiden kann, ob diese hohl oder gefüllt sind. Die Bartenwale, die kein Sonarsystem entwickelt haben, hören im niederen Frequenzbereich um 100 Hz und senden entsprechende Töne mit großer Lautstärke aus, die für Artgenossen über 100 km hörbar sind. Die Art der Lauterzeugung ist noch unklar, sehr wahrscheinlich werden die Töne in bestimmten Partien der Nasengänge gebildet. Gegen Lauterzeugung im Kehlkopf spricht das Fehlen von Stimmbändern. Die Blaslochmuskulatur wird vom Facialis -Nerv versorgt, dessen Kern neben der oberen Olive liegt. Als weitere Besonderheiten der Walgehirne wären dorsal noch das Fehlen der Epiphyse und ventral das Fehlen der Mammilarkörper zu nennen
4. Das Gegenbeispiel für progressive Hirnentwicklung im Wasser: die Seekühe
Zum Schluß noch kurz ein Blick auf die zweite rein marine Säugetiergruppe, die mit nur vier Arten an amerikanischen (Manatis) und asiatischen Küsten (Dugong) vertreten ist. Sie sind entfernt mit den Elefanten verwandt und leben als Pflanzenfresser in flachen Küstengewässern. Bei ihnen ist die Gehirnentwicklung deutlich anders verlaufen: das olfaktorische System ist nicht reduziert, das Gehirngewicht ist absolut und relativ auffallend gering, das Telencephalon ist kaum gefurcht und von ungewöhnlich weiten Ventrikeln durchzogen (Abbildung).
Empfohlene Literatur
AROYAN, J. L. (2001): Three-dimensional modeling of hearing in Delphinus delphis. J. Acoust. Soc. Am. 110, 3305-3318
BUTLER, A. B. u. W. HODOS (2005): Comparative Vertebrate Neuroanatomy. Evolution and Adaptation. John Wiley & Sons, Weinheim.
FRIEDL, W. A., P. E. NACHTIGALL, P. W. B. MOORE, N. K. W. CHUN, J. E. HAUN, R. W. HALL u. J. L. RICHARDS(1990): Taste Reception in the Pacific Bottlenose Dolphin (Tursiops truncatus Gilli) and the California Sea Lion (Zalophus Californianus). in: J. A. THOMAS u. R. A. KASTELEIN (Hrsg.): Sensory Abilities of Cetaceans; Laboratory and Field Evidence. Plenum Press, with Nato Scientific Affairs Division, N.Y., L., S. 447-454
GNONE, G., T. MORICONI u. G. GAMBINI (2006): Sleep behaviour: Activity and sleep in dolphins. Nature, Lond. 441, E10-E11
HAGNER, M. (2004): Geniale Gehirne. Zur Geschichte der Elitegehirnforschung. Wallstein Verlag, Göttingen.
HOF, P. R., R. CHANIS u. L. MARINO (2005): Cortical complexity in cetacean brains. Anat. Rec. A. Discov. Mol. Cell. Evol. Biol. 287A, 1142-1152
MANGER, P. R. (2006): An examination of cetacean brain structure with a novel hypothesis correlating thermogenesis to the evolution of a big brain. Biol. Rev. 81, 293-338
MARINO, L. (2004): Cetacean Brain Evolution: Multiplication Generates Complexity. IJCP 17, 1-16
MARINO, L., K. D. SUDHEIMER, W. A. MCLELLAN u. J. I. JOHNSON (2004): Neuroanatomical structure of the spinner dolphin (Stenella longirostris orientalis) brain from magnetic resonance images. Anat. Rec. A. Discov. Mol. Cell. Evol. Biol. 279, 601-610
MARINO, L., K. D. SUDHEIMER, D. A. PABST, W. A. MCLELLAN, S. ARSHAD, G. NAINI u. J. I. JOHNSON (2004): Anatomical Description of an Infant Bottlenose Dolphin (Tursiops truncatus) Brain from Magnetic Resonance Images. Aquatic Mammals 30, 315-326
MARINO, L., D. SOL, K. TOREN u. L. LEFEBVRE (2006): Does diving limit brain size in cetaceans? Mar. Mamm. Sci. 22, 413-425
RIDGWAY, S. H., D. HOUSER, J. J. FINNERAN, D. CARDER, M. KEOGH, W. VAN BONN, C. SMITH, M. SCADENG, D. DUBOWITZ, R. MATTREY u. C. HOH (2006): Functional imaging of dolphin brain metabolism and blood flow. J. Exp. Biol. 209, 2902-2910
OELSCHLÄGER, H. A. u. J. S. OELSCHLÄGER(2001): Brain. in: W. F. PERRIN, B. WÜRSIG u. J. G. M. THEWISSEN (Hrsg.): Encyclopedia of Marine Mammals. Academic Press, San Diego; 133-159, S.
WESTHEIDE, W. u. R. M. RIEGER (2003): Spezielle Zoologie. Teil 2: Wirbel- oder Schädeltiere. Spektrum Akademischer Verlag, Heidelberg.
Internet-Empfehlungen
The Navigable Atlas of the Dolphin Brain John I. Johnson, Lori Marino, Keith D. Sudheimer, Fabiano M.-Ferreira, D. Ann Pabst, William A. McLellan, James K. Rilling, Kristina K. Davis, Timothy L. Murphy, and Archibald J. Fobbs Jr. http://www.msu.edu/user/brains/turs/
RACICOT, R. u. M. COLBERT (2002): Tursiops truncatus, Bottlenose Dolphin. http://www.digimorph.org/specimens/Tursiops_truncatus/
MARINO, L. A., K. SUDHEIMER, T. L. MURPHY, K. K. DAVIS, D. A. PABST, W. MCCLELLAN, J. K. RILLING u. J. I. JOHNSON (2001): Anatomy and three-dimensional reconstructions of the bottlenose dolphin (Tursiops truncatus) brain from Magnetic Resonance Images. Anat. Rec. 264, 397-414 http://www.emory.edu/COLLEGE/ANTHROPOLOGY/FACULTY/ANTJR/Marino.pdf
Internet
Wally Welker, John Irwin Johnson, Adrianne Noe (2005):
Comparative Mammalian Brain Collections: Cetacea
http://brainmuseum.org/Specimens/cetacea/ (Stand 13.01.2005)
Anonymous (2005):
Bottle-nose dolphin (Tursiops truncatus) #66-127
http://brainmuseum.org/Specimens/cetacea/dolphin/index.html
(Stand 13.01.2005)
Rachel Racicot, Matthew Colbert (2002):
Tursiops truncatus, Bottlenose Dolphin, Digital Morphology
http://digimorph.org/specimens/Tursiops_truncatus/ (Stand 13.01.2005)
Caitlin Ramsey (2002):
Sonar In Dolphins. An exploration of the sonar system of Tursiops truncatushttp://instruct1.cit.cornell.edu/courses/bionb424/students/ckr5/neuroanatomy.html
(Stand 13.01.2005)


